Đốt cháy hoàn toàn 8,4 g hh A gồm : CH4 và C2H6 bằng không khí chứa 20% O2 và 80% N2 về thể tích ta thu đc 12,32 l khí CO2 đo ở đktc
Tính thể tích không khí cần dùng ở đktc?
Đốt cháy hoàn toàn 28 lít hỗn hợp khí gồm CH4 và C2H2 (trong đó CH4 chiếm 20% về thể tích). Hãy tính:
Thể tích không khí cần dùng (biết oxi chiếm 20% thể tích không khí)
Thể tích khí CO2 tạo thành. Biết các khí đều đo ở đktc.
Đốt cháy hoàn toàn 28 lít hỗn hợp gồm CH4 và C2H2 trong đó CH4 chiếm 20% về thể tích. Hãy tính
a) Thể tích không khí cần dùng biết oxi chiếm 20% thể tích không khí
b) Thể tích khí CO2 tạo thành biết các khí đều đo ở đktc
-----------------------------
CH4 chiếm 20% trong 28 lit hỗn hợp
=> V CH4 = 20%.28 = 5,6 lit
=> nCH4 = V/22,4 = 0,25 mol
=> V C2H2 = 28 - 5,6 = 22,4 lit
=> n C2H2 = V/22,4 = 1 mol
CH4 + 2O2 ---------> CO2 + 2H2O
0,25 0,5 0,25
C2H2 + 5/2O2 -------------> 2CO2 + H2O
1 2,5 2
=> V kh + 2,5).100/20.22,4 = 336 lit
=> VCO2 = (0,25 + 2).22,4 = 50,4 lit
Đốt cháy hoàn toàn V(lit) khi thiên nhiên ( có chứa 90% CH4 :5% C2H4,và 5% C2H8) cần dùng vừa đủ 246,4lit không khí ( có chứa 80% N2 và 20% O2) thu được khí CO2 và H2O
a) Tìm V?
b) Tính thể tích hỗn hợp khí thu được sau phản ứng
Biết các khí được đo ở cùng điều kiện về nhiệt độ và áp suất.
a) Giả sử các khí được đo ở điều kiện sao cho 1 mol khí chiếm thể tích 1 lít
Gọi số mol hỗn hợp khí là a (mol) => \(\left\{{}\begin{matrix}n_{CH_4}=0,9a\left(mol\right)\\n_{C_2H_4}=0,05a\left(mol\right)\\n_{C_3H_8}=0,05a\left(mol\right)\end{matrix}\right.\)
\(n_{O_2}=\dfrac{246,4.20\%}{1}=49,28\left(mol\right)\)
=> \(n_{N_2}=\dfrac{246,4}{1}-49,28=197,12\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,9a->1,8a---->0,9a--->1,8a
C2H4 + 3O2 --to--> 2CO2 + 2H2O
0,05a->0,15a------>0,1a-->0,1a
C3H8 + 5O2 --to--> 3CO2 + 4H2O
0,05a-->0,25a----->0,15a-->0,2a
=> 1,8a + 0,15a + 0,25a = 49,28
=> a = 22,4 (mol) => V = 22,4.1 = 22,4 (l)
b) Sau phản ứng thu được \(\left\{{}\begin{matrix}N_2:197,12\left(mol\right)\\CO_2:25,76\left(mol\right)\\H_2O:47,04\left(mol\right)\end{matrix}\right.\)
- Nếu H2O ở thể lỏng
=> hh khí gồm N2, CO2
=> \(V_{hh}=\left(197,12+25,76\right).1=222,88\left(l\right)\)
- Nếu H2O ở thể khí
=> hh gồm N2, CO2, H2O
=> \(V_{hh}=\left(197,12+25,76+47,04\right).1=269,92\left(l\right)\)
Đốt cháy hoàn toàn 7g hợp chất hữu cơ A thu được 11,2 l khí CO2 đo ở đktc và 9 g nước.
a, Xác định CTHH của A biết tỉ khối dA/CH4=1,75
b, Tính thể tích không khí cần dùng để đốt cháy hoàn toàn a biết oxi chiếm 20% không khí
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là:
A. 70,0 lít
B. 78,4 lít
C. 84,0 lít
D. 56,0 lít
Đáp án A
Hỗn hợp khí gồm CH4, C2H6 và C3H8 là các hidrocacbon.
Mà khi đốt cháy 1 hidrocacbon bất kì ta luôn có:
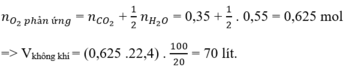
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là :
A. 78,4 lít
B. 56,0 lít
C. 70,0 lít
D. 84,0 lít
Đốt cháy hoàn toàn một thể tích khí thiên nhiêm gồm: metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là
A. 84,0 lít
B. 70,0 lít
C. 78,4 lít
D. 56,0 lít
Đốt cháy hoàn toàn mg hỗn hơp A cần vừa đủ 42 lít không khí. Sau phản ứng thu được 9gam nước và 44,8 lít hỗn hợp B gồm CO2 và N2. dB/H2=15. (Các khí đo ở đktc, không khí có 20%O2 và 80%N2 theo thể tích). Tính m và xác định công thức hóa học của A
Câu 8. Tì khối của một hỗn hợp khí gồm CH4 và C2H6 so với không khí bằng 0,6. a) Cần dùng bao nhiêu lít O2 để đốt cháy hoàn toàn 5,6 lít hỗn hợp đó. b) Tính khối lượng mỗi sản phẩm sinh ra.Biết các thể tích đo ở đktc
Gọi số mol CH4, C2H6 là a, b
=> a+b = \(\dfrac{5,6}{22,4}=0,25\)
Có \(\dfrac{16a+30b}{a+b}=0,6.29=17,4\)
=> a = 0,225; b = 0,025
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
____0,225->0,45------->0,225->0,45
2C2H6 + 7O2 --to--> 4CO2 + 6H2O
0,025->0,0875----->0,05-->0,075
=> VO2 = (0,45+0,0875).22,4 = 12,04 (l)
mCO2 = (0,225 + 0,05).44 = 12,1(g)
mH2O = (0,45+ 0,075).18 = 9,45(g)
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là
A. 70,0 lít
B. 84,0 lít
C. 56,0 lít.
D. 78,4 lít.